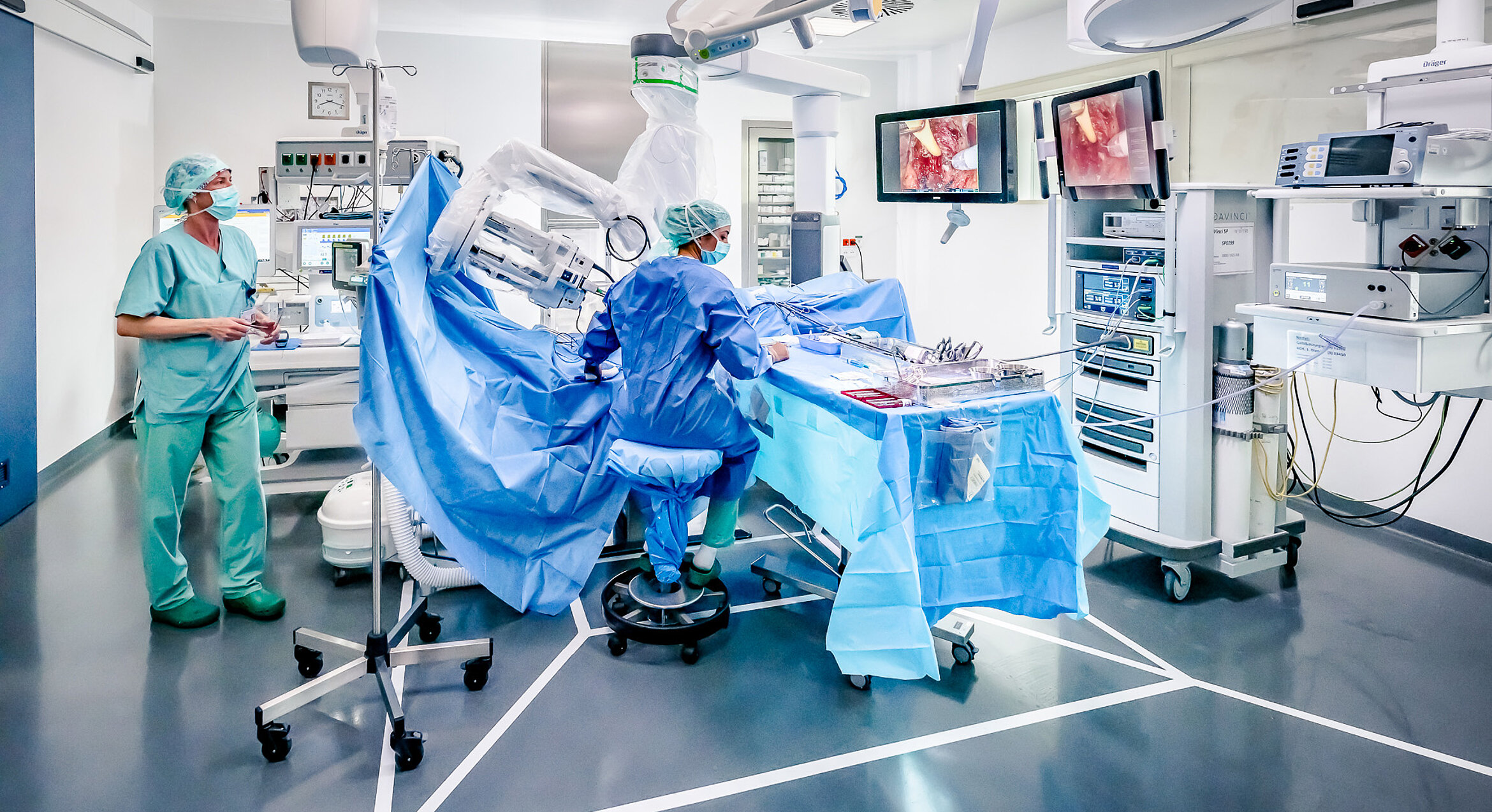
Die FFLU-Technik
Um eine Inkontinenz nach Prostatektomie möglichst zu vermeiden, haben wir die FFLU-Operationstechnik (Full-Functional-Length-Uretha) entwickelt, mit der die Funktionstüchtigkeit des Harnröhrenschließmuskels komplett erhalten bleiben kann. Dabei wird die Harnröhre so präpariert, dass der Schließmuskel vollständig, in kompletter funktioneller Länge erhalten bleibt und seine anatomische einwandfreie Lage im Beckenboden rekonstruiert wird.
Anatomische und funktionelle Studien haben gezeigt, dass die Länge der funktionellen (membranösen) Urethra lediglich zwischen 1,5 und 4 cm beträgt. Im Embryonalstadium reichen die Sphinktermuskelfasern direkt bis an die Harnblase. Die Prostata entwickelt sich aus einer Harnröhrenknospe und nimmt dann in der weiteren Entwicklung den Raum zwischen Harnblase und Sphinkter ein, wobei sie den quergestreiften Anteil des Sphinkters mit dem Apex verdrängt. An anatomischen Präparaten und teilweise auch bei der radikalen Prostatektomie können die residualen Muskelfasern (Detrusor apron) an der ventralen Prostata bis hin zur Blase identifiziert werden. Die Apexform kann sehr stark zwischen einzelnen Individuen variieren, sodass apikales Prostatagewebe je nach Ausprägung zwischen 10 und 40 % des muskulären Sphinkters umschließt.
Die Apexform beeinflusst die postoperative Kontinenz
In einer MRT-Studie konnten Lee et al. 2006 einen signifikanten Einfluss der Apexform auf die postoperative Kontinenz nachweisen. Aufgrund dieser Studienergebnisse und eigener anatomischer Beobachtungen haben wir unsere Operationstechnik modifiziert, um bei jedem Patienten unabhängig von der individuellen Apexanatomie die komplette muskuläre Harnröhre zu erhalten.
Neben der funktionellen Länge des Sphinkters spielt die anatomische und statische Fixierung der Harnröhre im Beckenboden eine wichtige Rolle. Als Ringmuskel kann der Sphinkter seine maximale Kraft nur entfalten, wenn er über die gesamte Länge am Beckenboden fixiert ist. Weiterhin können auch geringe Deviationen der Harnröhre eine Inkontinenz auslösen. Der posteriore Anteil des Sphinkters ist durch ein Bindegewebsband (mediale dorsale Gewebebrücke) über den Musculus rectourethralis am Beckenboden fixiert. Die puboperinealen Anteile des rechten und linken Musculus levator ani (M. puboperinealis oder Levator urethrae) inserieren in die mediane Gewebebrücke und bilden hierdurch eine Schlinge um die Harnröhre.
Die Müller‘schen Ligamente (Ligamenta ischioprostatica) sind eine wichtige anatomische Leitstruktur. Sie stabilisieren außerdem die Harnröhre lateral. Die Müller‘schen Bänder stellen eine Verdickung der Faszie des externen quergestreiften Sphinkters dar. Sie trennen anatomisch den Bereich des dorsalen Venenplexus vom Beginn des Gefäßnervengewebes und sind deshalb eine wichtige anatomische Leitstruktur. Um die komplette Zirkumferenz des Sphinkters sowie des umgebenden dorsalen Venenplexus darzustellen, präpariert der Operateur die kranialen Anteile der beiden Mm.levator urethrae sorgfältig nach kaudal.
Meistens ist der M. levator urethrae locker mit dem Apex verbunden, sodass der Operateur ihn stumpf vom Apex abpräparieren kann. Die untere Fixierung der Harnröhre am medialen Gewebeband sollte vor der Durchtrennung des dorsalen Venenplexus dargestellt werden, um die Ausdehnung des proximalen (unter der Harnröhre gelegenen) Anteils des Apex abschätzen zu können. Die Durchtrennung des dorsalen Venenplexus erfolgt direkt über dem Apex, indem der Operateur die Prostata nach kaudal und proximal leicht mit einem Stiel mobilisiert.
Die Faszie des äußeren, quergestreiften Spinkters sollte voll intakt bleiben
Bei der Durchtrennung des Plexus sollte man darauf achten, die Faszie des äußeren, quergestreiften Sphinkters zugunsten der Physiologieerhaltung intakt zu lassen. Den dorsalen Venenplexus sollte der Operateur streng bis zu den Müller‘schen Bändern durchtrennen. Nach selektiver Umstechung des dorsalen Venenplexus kann man nun den muskulären intraprostatischen Harnröhrenanteil entlang der Müller‘schen Bänder als anatomische Leitstruktur präparieren, indem das locker über der Harnröhre lokalisierte apikale Gewebe stumpf nach kaudal präpariert wird.
Es ist wichtig anzumerken, dass das den intraprostatischen Sphinkter umkleidende Gewebe nicht mit dem Schließmuskel verwachsen ist. Dieses Gewebe besteht hauptsächlich aus apikalem Prostataparenchym, Resten des dorsalen Venenplexus sowie dem Detrusor apron. Unsere eigenen Studien haben gezeigt, dass die sorgfältige Präparation dieses Gewebes keinen onkologisch negativen Einfluss hat, solange die Präparation streng nach anatomischen Leitstrukturen erfolgt.
Die Präparation der dorsalen Harnröhre erfolgt nach der Platzierung der ventralen und lateralen Anastomosennähte. Die posteriore Harnröhrenschleimhaut wird kranial des Colliculus scharf inzidiert und die Schleimhaut stumpf, z.B. mit einer geschlossenen feinen Schere, nach kaudal geschoben. Hierbei wird dann der längsgestreifte Anteil des Sphinkters sichtbar und lässt sich in der Regel ohne scharfe Präparation bis zu seiner kranialen Begrenzung darstellen und durchtrennen.
Nach diesem Manöver sind die längsgestreiften Muskel fasern in der Regel noch durch Bindegewebsstränge mit den posterioren Anteilen des Apex verbunden. Diese kann man unter Sicht sicher durchtrennen, und der Apex ist dann komplett nach anterior zu mobilisieren. Durch diese stringente anatomische Präparation bleibt die posteriore Fixierung der Harnröhre komplett erhalten, sodass der Sphinkter seine Kraft auf voller Länge entfalten kann.